La thérapie génique peut avoir le potentiel de réparer ou de remplacer les mutations génétiques, qui sont des changements dans votre ADN qui affectent le fonctionnement de votre corps.
Les médecins utilisent la thérapie génique, également appelée « édition de gènes », pour modifier directement vos gènes.
Cette approche peut aider à traiter les maladies causées par une seule mutation, telles que la bêta-thalassémie ou l’amyotrophie spinale (SMA). L’édition de gènes peut également aider à traiter certains cancers.
Les outils d’édition de gènes tels que CRISPR-Cas9 sont très récents et évoluent rapidement. Les chercheurs continuent d’étudier leur plein potentiel ainsi que les risques qu’ils peuvent poser.
Voici ce que les experts savent jusqu’à présent sur la thérapie génique.
Les gènes sont de petits segments d’ADN qui ordonnent à vos cellules de fabriquer certaines protéines lorsque des conditions spécifiques sont remplies.
Les gènes mutés, en revanche, peuvent amener vos cellules à fabriquer trop ou trop peu de protéines nécessaires. Même de petits changements peuvent avoir un effet domino sur tout votre corps, tout comme de minuscules changements dans le code informatique peuvent affecter un programme entier.
La thérapie génique peut résoudre ce problème par:
- remplacer un gène manquant ou « cassé » par une copie de travail
- désactiver les gènes défectueux
- ajouter des gènes aux cellules immunitaires pour les aider à mieux cibler les cellules malades
Vecteurs viraux
Les scientifiques n’ont pas de pincettes assez petites pour éditer votre ADN à la main. Au lieu de cela, ils recrutent un allié surprenant pour travailler en leur nom : les virus.
En règle générale, un virus pénètre dans vos cellules et modifie votre ADN pour créer davantage de copies de lui-même. Mais les scientifiques peuvent remplacer cette programmation par la leur, détournant le virus pour guérir au lieu de nuire. Celles-ci vecteurscomme on les appelle, n’ont pas les parties dont ils ont besoin pour causer la maladie, ils ne peuvent donc pas vous rendre malade comme le ferait un virus ordinaire.
Il existe deux types de thérapie génique :
- In vivo (à l’intérieur de votre corps) : Les scientifiques placent le vecteur transportant les nouveaux gènes directement dans votre corps via une injection ou une perfusion intraveineuse (IV).
- Ex vivo (hors de votre corps) : Les scientifiques extraient des cellules de votre corps et les présentent au vecteur dans une boîte de Pétri. Ensuite, vos cellules modifiées sont renvoyées dans votre corps, où elles se multiplieront, espérons-le.
Chaque type a le sien avantages:
La thérapie génique est différente du génie génétique, qui consiste à modifier un ADN autrement sain dans le but d’améliorer des traits spécifiques. En théorie, le génie génétique pourrait potentiellement réduire le risque de certaines maladies chez un enfant ou changer la couleur de ses yeux. Mais la pratique reste très controversé puisqu’il est très proche de l’eugénisme.
La thérapie génique peut être utilisée pour traiter une variété de maladies génétiques, notamment :
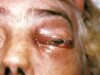
Perte de vision héréditaire
Lorsque le gène RPE65 dans vos rétines ne fonctionne pas, vos globes oculaires ne peuvent pas convertir la lumière en signaux électriques.
La thérapie génique Luxturna, approuvée par la Food and Drug Administration (FDA) en 2017peut fournir un remplacement fonctionnel du gène RPE64 à vos cellules rétiniennes.
Troubles sanguins
Les Approuvé par la FDAHemgenix peut traiter le trouble de la coagulation hémophilie B. Le vecteur viral demande à vos cellules hépatiques de créer davantage de protéine facteur IX, qui aide votre sang à coaguler.
Pendant ce temps, la thérapie génique Zynteglo, approuvée par la FDA en 2022traite la bêta-thalassémie en donnant aux cellules souches de la moelle osseuse des instructions correctes pour créer de l’hémoglobine.
Ce trouble sanguin peut réduire l’oxygène dans votre corps car il diminue la production d’hémoglobine de votre corps.
Amyotrophie spinale (SMA)
Dans la SMA infantile, le corps d’un nourrisson ne peut pas fabriquer suffisamment de protéines de « survie des motoneurones » (SMN) nécessaires à la construction et à la réparation des motoneurones. Sans ces neurones, les nourrissons perdent progressivement leur capacité à bouger et à respirer.
La thérapie génique Zolgensma, approuvée par la FDA en 2019remplace les gènes SMN1 défectueux dans les cellules motrices d’un nourrisson par des gènes capables de créer suffisamment de protéines SMN.
Adrénoleucodystrophie cérébrale (CALD)
Votre gène ABCD1 produit une enzyme qui décompose les acides gras dans votre cerveau. Si vous souffrez d’adrénoleucodystrophie cérébrale, ce gène est cassé ou manquant.
Skysonaapprouvé par la FDA à partir de 2022, délivre un gène ABCD1 fonctionnel afin que les acides gras ne s’accumulent pas et ne causent pas de lésions cérébrales.
Cancers
La FDA a approuvé les thérapies géniques pour traiter plusieurs types de cancer, tels que le lymphome non hodgkinien et le myélome multiple.
La plupart des thérapies géniques anticancéreuses fonctionnent indirectement en insérant de nouveaux gènes dans un puissant anticorps appelé cellule T. Vos cellules T modifiées peuvent alors s’accrocher aux cellules cancéreuses et les éliminer, de la même manière qu’elles attaquent les virus.
La thérapie Adstiladrineapprouvé par la FDA en 2022peut traiter le cancer de la vessie non invasif sur le plan musculaire en modifiant l’ADN des cellules de votre vessie elles-mêmes.
Certaines personnes qui envisagent une thérapie génique peuvent se sentir mal à l’aise à l’idée de mettre des virus dans leur corps.
Gardez à l’esprit, cependant, que les thérapies géniques subissent des tests approfondis avant d’être approuvées. Les virus des thérapies géniques sont également fixés afin qu’ils ne puissent pas se répliquer, comme de nombreux vaccins.
Cela dit, les thérapies géniques peuvent présenter d’autres risques :
- Réponse immunitaire: Votre système immunitaire peut confondre les vecteurs viraux avec une menace envahissante. L’afflux de globules blancs qui en résulte peut déclencher des effets secondaires comme la fièvre, l’inflammation et la fatigue.
- Montage hors cible : Il existe un risque que le vecteur viral insère son paquet génétique dans le mauvais tronçon d’ADN, créant essentiellement une nouvelle mutation. Dans un cas en 2002, de telles mutations ont conduit au cancer. Cela dit, les scientifiques ont depuis développé des vecteurs « plus intelligents » qui font moins d’erreurs de ciblage.
- Effets à long terme inconnus : Parce que les thérapies géniques sont si nouvelles, les scientifiques ne savent pas encore comment elles pourraient affecter votre corps à long terme. Certains experts ont exprimé des préoccupations que les vecteurs viraux peuvent transmettre des mutations à la génération suivante s’ils éditent accidentellement des ovules ou des spermatozoïdes.
Malgré ces problèmes, les experts pensent généralement que la thérapie génique offre plus d’avantages que de risques.
La plupart des affections traitées par thérapie génique mettent la vie en danger. Les dangers de les laisser non traités l’emportent souvent sur les risques d’effets secondaires potentiels.
La thérapie génique présente quelques inconvénients qui l’empêchent de devenir un traitement répandu.
Cibles limitées
La thérapie génique ne peut cibler que certaines mutations. Cela signifie que cela peut ne pas fonctionner pour tout le monde avec une condition spécifique.
Par exemple, deux personnes peuvent avoir hérité d’une perte de vision. Actuellement, la thérapie génique ne peut traiter que la perte de vision causée par la mutation RPE64.
Temps à l’approbation
Parce que la recherche sur la thérapie génique est si nouvelle, les experts effectuent des tests de sécurité approfondis avant de présenter leurs traitements au public. Ça peut prendre des années obtenir l’approbation de la FDA pour chaque nouvelle thérapie.
Frais
Comme vous pouvez l’imaginer, les thérapies géniques sont coûteuses à fabriquer et à administrer. Cela affecte non seulement le financement des essais cliniques, mais également le prix du médicament.
Par exemple, la thérapie génique Zolgensma est le médicament le plus cher aux États-Unis à 2,1 millions de dollars par dose. Même avec une assurance, ce genre de prix reste hors de portée pour l’Américain moyen.
Les scientifiques tentent de trouver des moyens de rendre le processus de développement plus sûr, moins cher et plus efficace afin que davantage de personnes puissent accéder à la thérapie génique.
La thérapie génique permet de traiter plusieurs maladies génétiques différentes en modifiant les mutations qui les provoquent. Au fur et à mesure que les chercheurs affinent et étendent cette technologie, ils pourraient trouver encore plus de conditions qui pourraient être traitées avec.
Les experts continuent également d’explorer des options pour rendre la thérapie génique plus abordable afin que les personnes qui ont besoin de ces traitements aient plus de facilité à les obtenir.
Emily Swaim est une rédactrice et rédactrice indépendante spécialisée en psychologie. Elle est titulaire d’un baccalauréat en anglais du Kenyon College et d’une maîtrise en écriture du California College of the Arts. En 2021, elle a reçu sa certification Board of Editors in Life Sciences (BELS). Vous pouvez trouver plus de son travail sur GoodTherapy, Verywell, Investopedia, Vox et Insider. Retrouvez-la sur Twitter et LinkedIn.