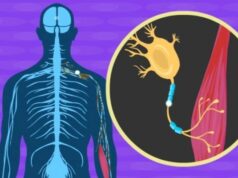
- Faiblesse ou paralysie des muscles du pied et du bas de la jambe, pouvant entraîner des difficultés à lever le pied (pied tombant)
- Une démarche rapide avec des trébuchements ou des chutes fréquentes
- Problèmes d’équilibre
- Déformations du pied, telles que voûtes plantaires hautes et orteils recourbés (orteils en marteau)
- Le bas des jambes peut prendre la forme d’une « bouteille de champagne inversée » en raison de la perte de volume musculaire.
- Capacité réduite à ressentir la chaleur, le froid et le toucher
- Une faiblesse et une atrophie peuvent survenir dans les mains, entraînant des difficultés avec la motricité fine.
- Diminution du sens des vibrations et de la position (proprioception)
- Courbure de la colonne vertébrale (scoliose)
- Déplacement de la hanche
- Contractures (raccourcissement chronique des muscles ou des tendons autour des articulations)
- Crampes musculaires
- Douleur névralgique
une innovation thérapeutique 100 % française à base d’ARN
En biologie moléculaire, la transcription correspond à la copie d’une molécule d’ADN en une molécule d’ARN. Cette molécule d’ARN est ensuite « traduite » en une protéine, qui peut assurer différentes fonctions au sein des cellules de l’organisme. Lorsque qu’une protéine particulière, appelée PMP22, est fabriquée en quantité deux fois plus importante que la normale, elle provoque le développement de la maladie génétique Charcot-Marie Tooth de type 1A. Cette surproduction entraine une paralysie progressive des jambes et des mains. Tout l’enjeu est donc de réussir à normaliser l’expression de cette protéine chez les personnes atteintes de la maladie de Charcot-Marie Tooth. Pour cela, des scientifiques français ont mis au point une thérapie, brevetée2 , fondée sur la dégradation de l’ARN codant pour la protéine PMP22. Ils ont utilisé à cette fin d’autres petits ARN capables d’interférer avec un ARN spécifique, ici celui codant pour la PMP22, et de conduire à sa dégradation ou à la diminution de sa traduction en protéine. La difficulté pour la mise au point de cette thérapie a été de stabiliser ces petits ARN, dit interférents (ou siARN), qui se dégradent très rapidement dans l’environnement biologique. Les chercheuses et chercheurs les ont couplés avec une autre molécule, le squalène, classiquement utilisée en cosmétologie ou en pharmacologie. Biocompatible, biodégradable et formant dans l’eau des nanoparticules, le squalène protège les siARN de toute dégradation. Il permet également de contrôler la taille des particules formées et la quantité de siARN injectée. Les scientifiques ont ensuite montré, sur des souris modèles de cette maladie, que l’injection de ces ARN interférents permettait la restitution complète et rapide de l’activité locomotrice et de la force des souris. Les ARN pénètrent dans les nerfs périphériques, renforcent la couche de myéline3 autour de ces nerfs et normalisent la vitesse du signal nerveux. L’effet du traitement perdure trois semaines pour les formes graves et plus de dix semaines pour les formes plus légères de la maladie. Cette stratégie thérapeutique pour les neuropathies périphériques héréditaires, entièrement mise au point en France, constitue la preuve de concept d’une nouvelle médecine de précision fondée sur la normalisation par siARN de l’expression d’un gène surexprimé. Elle reste à développer chez l’humain avec des études pré-cliniques et cliniques.